Công thức phân tử: C2H4O2.
Phân tử khối: 60.
I. TÍNH CHẤT VẬT LÍ
- Axit axetic C2H4O2 là chất lỏng, không màu, vị chua, tan vô hạn trong nước.
- Dung dịch axit axetic nồng độ từ 2 – 5 % dùng làm giấm ăn.
- Giấm có tối thiểu 4% acid acetic theo thể tích.Điều đó khiến acid acetic là thành phần chính trong giấm ngoài nước. Acid acetic có vị chua dễ nhận biết và mùi đặc trưng.
- Giấm được điều chế bằng cách lên men rượu etylic. Axit axetic còn có thể được điều chế từ acetylen, cracking dầu mỏ hoặc chưng cất gỗ.
II. CẤU TẠO PHÂN TỬ
Công thức cấu tạo:
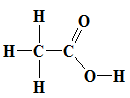
- Viết gọn CH3-COOH hay CH3COOH.
- Do phân tử có nhóm -COOH nên phân tử có tính axit.
III. TÍNH CHẤT HÓA HỌC
1. Axit axetic mang đầy đủ tính chất của một axit
- Axit axetic là một axit yếu, yếu hơn các axit HCl, H2SO4, HNO3. Nhưng axit axetic có đầy đủ tính chất của một axit.
CH3COOH + NaOH → H2O + CH3COONa
2. Axit axetic tác dụng với rượu etylic tạo etyl axetat
C2H5OH + CH3COOH → CH3COOC2H5 + H2O ( xúc tác H2SO4 đặc, nhiệt độ)
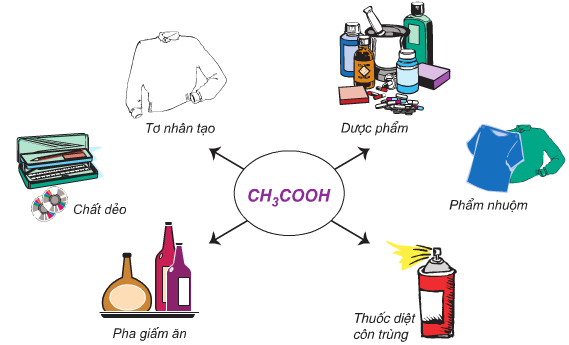
IV. ỨNG DỤNG
V. ĐIỀU CHẾ
- Để sản xuất giấm ăn, thường dùng phương pháp lên men dung dịch rượu etylic loãng.
CH3CH2OH + O2 → CH3COOH + H2O. (xúc tác men giấm)

.jpg)
.jpg)




.jpg)
.jpg)










